I. DEFINIŢIA AFECŢIUNII
Mielomul multiplu (MM)
II. CRITERII DE INCLUDERE ÎN TRATAMENTUL SPECIFIC
Ixazomib, în asociere cu lenalidomidă şi dexametazonă, este indicat pentru tratamentul pacienţilor adulţi
cu mielom multiplu care au urmat cel puţin un tratament anterior.
III. CRITERII DE EXCLUDERE
– hipersensibilitatea la substanţa activă sau la oricare dintre excipienţi
– deoarece ixazomib se administrează în asociere cu lenalidomidă şi dexametazonă, pentru
contraindicaţii suplimentare consultaţi RCP aferent acestor medicamente.
– sarcina şi alăptarea
IV. DOZE ŞI MOD DE ADMINISTRARE
Tratamentul trebuie iniţiat şi monitorizat sub supravegherea unui medic cu experienţă în tratamentul
mielomului multiplu.
Doze
Doza iniţială recomandată de ixazomib este 4 mg, administrată pe cale orală o dată pe săptămână, în
zilele 1, 8 şi 15 ale unui ciclu de tratament de 28 de zile.
Doza iniţială recomandată de lenalidomidă este 25 mg, administrată zilnic în zilele 1 – 21 ale unui ciclu de
tratament de 28 de zile.
Doza iniţială recomandată de dexametazonă este 40 mg, administrată în zilele 1, 8, 15 şi 22 ale unui ciclu
de tratament de 28 de zile.
Schema de administrare: ixazomib administrat în asociere cu lenalidomidă şi dexametazonă
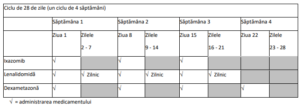
Pentru informaţii suplimentare privind lenalidomida şi dexametazona, consultaţi rezumatul
caracteristicilor produsului (RCP) aferent acestor medicamente.
Înainte de iniţierea unui nou ciclu de tratament:
– Numărul absolut de neutrofile trebuie să fie ≥ 1.000/mm3
– Numărul de trombocite trebuie să fie ≥ 75.000/mm3
– În general, în caz de toxicitate non-hematologică, starea pacientului ar trebui să revină la cea
iniţială sau ≤ gradul 1, la latitudinea medicului.
Tratamentul trebuie continuat până la evoluţia bolii sau până la toxicitate inacceptabilă.
Tratamentul cu ixazomib în asociere cu lenalidomidă şi dexametazonă pe o durată mai mare de 24 de
cicluri trebuie să aibă ca bază evaluarea individuală a raportului beneficiu-risc, deoarece datele privind
toleranţa şi toxicitatea pe o perioadă mai lungă de 24 de cicluri sunt limitate.
Doze întârziate sau omise
În cazul în care o doză de ixazomib este întârziată sau omisă, doza trebuie administrată numai dacă
următoarea doză este programată la o distanţă de ≥ 72 de ore. O doză omisă nu trebuie administrată cu
mai puţin de 72 de ore înainte de următoarea doză programată. Nu trebuie administrată o doză dublă
pentru a compensa doza omisă.
Dacă un pacient vomită după administrarea unei doze, nu trebuie să ia din nou doza, ci trebuie să reia
administrarea la momentul următoarei doze programate.
Modificări de doză
Etapele de reducere a dozei de ixazomib sunt prezentate în Tabelul 1, iar îndrumările de modificare a
dozei sunt furnizate în Tabelul 2.
Tabelul 1: Etapele de reducere a dozei de ixazomib

*) Doza redusă recomandată de 3 mg în prezenţa insuficienţei hepatice moderate sau severe, insuficienţei renale severe
sau bolii renale în stadiu terminal (BRST) care necesită dializă.
Se recomandă o abordare alternantă a modificării dozei pentru ixazomib şi lenalidomidă, din cauza
suprapunerii toxicităţilor care determină trombocitopenie, neutropenie şi erupţie cutanată. Din cauza acestor
toxicităţi, prima etapă în modificarea dozei este aceea de a reduce doza de lenalidomidă/înceta administrarea
acesteia. Consultaţi RCP aferent lenalidomidei, pentru etapele de reducere a dozei pentru aceste toxicităţi.
Tabelul 2: Ghid de modificare a dozei pentru ixazomib în asociere cu lenalidomidă şi dexametazonă
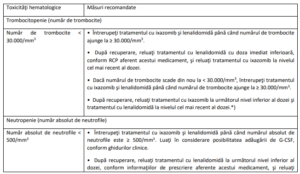
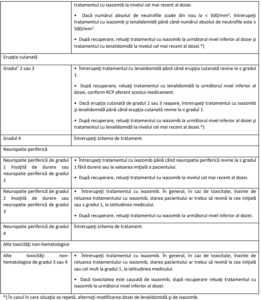
Clasificare pe baza criteriilor terminologice uzuale ale Institutului Naţional pentru Cancer (National
Cancer Institute) (CTCAE) versiunea 4.03.
V. MONITORIZARE:
La iniţierea terapiei şi periodic (fie lunar, fie la aprecierea medicului):
– criteriile IMWG de evaluare a bolii
– examen clinic
– monitorizat pentru depistarea simptomelor de neuropatie periferică
– hemoleucograma completă
– coagulograma
– probe hepatice (transaminaze, bilirubina)
– probe renale
– electroliţi
PRECAUŢII ŞI ATENŢIONĂRI:
Deoarece ixazomib se administrează în asociere cu lenalidomidă şi dexametazonă, pentru informaţii
suplimentare privind atenţionările şi precauţiile speciale pentru utilizare consultaţi RCP aferent acestor
medicamente.
Trombocitopenie
A fost raportată trombocitopenia în asociere cu ixazomib, cea mai mică valoare a numărului de
trombocite fiind atinsă de regulă între zilele 14 – 21 ale fiecărui ciclu de 28 de zile, iar revenirea la valorile
iniţiale având loc până la începutul următorului ciclu.
În timpul tratamentului cu ixazomib numărul de trombocite trebuie monitorizat cel puţin lunar. În
primele trei cicluri trebuie luată în considerare monitorizarea mai frecventă, conform RCP aferent
lenalidomidei. Trombocitopenia poate fi tratată prin modificarea dozei şi transfuzii de masă
trombocitară, conform ghidurilor medicale standard.
Toxicităţi gastro-intestinale
Au fost raportate diaree, constipaţie, greaţă şi vărsături în asociere cu ixazomib, care ocazional necesită
utilizarea de medicamente antiemetice şi antidiareice şi tratament de susţinere. Doza trebuie ajustată
pentru simptome severe (gradul 3 – 4). În caz de evenimente gastro-intestinale severe se recomandă
monitorizarea concentraţiei serice de potasiu.
Neuropatie periferică
A fost raportată neuropatie periferică în asociere cu ixazomib. Pacientul trebuie monitorizat pentru
depistarea simptomelor de neuropatie periferică. Pacienţii care prezintă neuropatie periferică nou
instalată sau care se agravează pot necesita modificarea dozei.
Edem periferic
A fost raportat edem periferic în asociere cu ixazomib. Pacientul trebuie evaluat pentru depistarea
cauzelor subiacente şi, dacă este necesar, trebuie să i se asigure asistenţă medicală de susţinere. Doza de
dexametazonă trebuie ajustată conform informaţiilor de prescriere aferente acesteia sau ixazomib
pentru simptome de gradul 3 sau 4.
Reacţii cutanate
A fost raportată erupţie cutanată în asociere cu ixazomib. Erupţia cutanată trebuie tratată prin măsuri de
susţinere sau prin modificarea dozei, dacă este de gradul 2 sau mai mare.
Hepatotoxicitate
Au fost raportate mai puţin frecvent leziuni hepatice induse de medicament, leziuni hepatocelulare,
steatoză hepatică, hepatită colestatică şi hepatotoxicitate în asociere cu ixazomib. Este necesară
monitorizarea periodică a nivelului enzimelor hepatice, iar doza trebuie ajustată pentru simptome de
gradul 3 sau 4.
Sarcina
Femeile trebuie să evite să rămână gravide în timpul tratamentului cu ixazomib. Dacă se utilizează
ixazomib în timpul sarcinii sau dacă pacienta rămâne gravidă în timpul tratamentului cu ixazomib,
aceasta trebuie să fie informată cu privire la riscurile potenţiale pentru făt.
Femeile aflate la vârsta fertilă trebuie să utilizeze măsuri contraceptive extrem de eficace în timpul
administrării ixazomib şi timp de 90 de zile după încetarea tratamentului. Femeile care utilizează
contraceptive hormonale trebuie să utilizeze suplimentar o metodă contraceptivă de tip barieră.
Sindrom de encefalopatie posterioară reversibilă
Sindromul de encefalopatie posterioară reversibilă (SEPR) a apărut la pacienţi cărora li s-a administrat
ixazomib. SEPR este o tulburare neurologică rară, reversibilă, care se poate manifesta prin convulsii,
hipertensiune arterială, cefalee, conştienţă modificată şi tulburări de vedere. Pentru confirmarea
diagnosticului se utilizează o metodă de imagistică cerebrală, preferabil imagistică prin rezonanţă
magnetică. La pacienţii la care apare SEPR, tratamentul cu ixazomib trebuie întrerupt.
Inductori puternici ai CYP3A
Inductorii puternici pot reduce eficacitatea ixazomib; prin urmare, trebuie evitată utilizarea
concomitentă a inductorilor puternici ai CYP3A, cum sunt carbamazepina, fenitoina, rifampicina şi
sunătoarea (Hypericum perforatum). Dacă administrarea concomitentă a unui inductor puternic al
CYP3A nu poate fi evitată, monitorizaţi îndeaproape pacienţii pentru ţinerea bolii sub control.
REACŢII ADVERSE (Tabelul 3):
Tabelul 3: Reacţii adverse la pacienţii trataţi cu ixazomib în asociere cu lenalidomidă şi dexametazonă (toate
gradele, gradul 3 şi gradul 4)
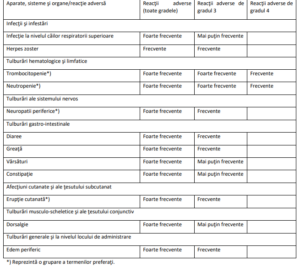
Notă: reacţiile adverse la medicament incluse sub forma termenilor preferaţi se bazează pe MedDRA versiunea 16.0.
CRITERII DE EVALUARE A EFICACITĂŢII TERAPEUTICE
Se utilizează criteriile elaborate de către Grupul Internaţional de Lucru pentru Mielom (IMWG). (Tabelul
4):
Tabelul 4
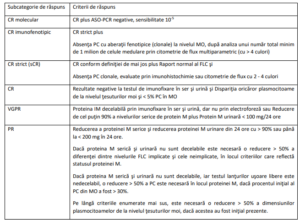
PC = plasmocite; MO = măduvă osoasă; CR = răspuns complet; VGPR = răspuns parţial foarte bun; PR = răspuns parţial;
ASO-PCR = reacţia în lanţ a polimerazei, specifică anumitor alele; FLC = lanţuri uşoare libere.
VI. PRESCRIPTORI
Iniţierea şi continuarea tratamentului se face de către medicii din specialitatea hematologie (sau, după
caz, specialişti de oncologie medicală).
Autor: FormareMedicala.ro









