1. INTRODUCERE
I.1. Definiţie/Nomenclatură
Vasculitele ANCA pozitive sunt un grup heterogen de boli cu manifestări clinice multisistemice,
caracterizate prin inflamaţia necrotică pauci-imună a peretelui vaselor mici definite ca artere mici
intraparenchimatoase, arteriole, capilare şi venule şi asociate cu prezenţa de anticorpi circulanţi antineutrophil cytoplasmic antibodies (ANCA) în aproximativ 80 – 96% dintre pacienţi.
În conformitate cu 2012 Revised International Chapel Hill Consensus Conference Nomenclature
of Vasculitidis, vasculitele ANCA pozitive I următoarele entităţi clinico-patologice:
– granulomatoza cu poliangiită (GPA), fostă Wegener, care asociază vasculită necrotică a vaselor
mici şi uneori medii, cu puţine sau fără depozite imune, inflamaţie granulomatoasă necrotică a
tractului respirator şi inferior, glomerulonefrita necrotică pauci-imună fiind frecventă;
– poliangiita microscopică (PAM), caracterizată prin glomerulonefrită necrotică şi frecventă
capilarită pulmonară în asociere cu vasculită necrotică a vaselor mici şi uneori medii, cu puţine
sau fără depozite imune în absenţa inflamaţiei granulomatoase;
– granulomatoza eozinofilică cu poliangiită (GEPA), fostă Churg-Strauss, care asociază vasculită
necrotică a vaselor mici şi uneori medii, cu puţine sau fără depozite imune, inflamaţie
granulomatoasă necrotică şi bogată în eozinofile, alături de astm, polipi nazali şi eozinofilie,
ANCA întâlnindu-se mai frecvent când este prezentă glomerulonefrita;
– vasculita ANCA pozitivă limitată la un singur organ (de exemplu vasculita ANCA pozitivă
limitată renal).
Ţintele antigenice principale pentru ANCA sunt proteinaza 3 (PR3) cu aspect citoplasmatic (c-ANCA)
şi mieloperoxidaza (MPO) cu aspect perinuclear (p-ANCA) la imunofluorescenţă indirectă (IFI), aceste
antigene fiind prezente în granulele neutrofilelor şi în lizozomii macrofagelor, activarea lor prin
autoanticorpi specifici inducând activarea celulară şi distrucţia peretelui vascular. Alte proteine
intracelulare neutrofilice care pot fi ţinte pentru ANCA sunt reprezentate de elastaza, cathepsina G,
lactoferina şi lizozimul.
Date recente consideră că definirea vasculitelor ANCA pozitive pe baza celor 2 antigene ţintă în
vasculite PR3-ANCA pozitive şi vasculite MPO-ANCA pozitive defineşte mai bine grupe omogene de
pacienţi decât elementele clinico-patologice prezentate şi lasă loc pentru vasculitele ANCA negative (XANCA), în care noi ANCA nu sunt încă identificaţi.
Există frecvenţe diferite a PR3-ANCA şi MPO-ANCA în diferitele tipuri de vasculite ANCA
pozitive. Astfel, 65% dintre pacienţii cu GPA au PR3-ANCA şi 20% au MPO-ANCA. Date recente
arată că factori genetici, factori de mediu, cum sunt infecţiile bacteriene, virale, parazitare, medicamente
(ex. Propiltiouracil) şi siliciu au fost implicaţi în pozitivitatea ANCA.
I.2. Epidemiologie
Vasculitele ANCA pozitive sunt boli rare, dar foarte severe, ele fiind asociate cu morbiditate şi
mortalitate crescute secundare evoluţiei ciclice cu remisiuni şi recăderi şi reacţiilor adverse secundare
medicaţiei utilizate. Fără tratament, vasculitele ANCA pozitive sunt fatale în 90% dintre cazuri.
În cadrul grupului vasculitelor ANCA pozitive, GPA şi PAM sunt cele mai frecvente (90%),
GEPA fiind cea mai rară (10%) şi, din acest motiv, deşi preocupările terapeutice sunt mai consistente în
formele frecvente, abordările terapeutice sunt identice. Ratele de incidenţă anuală pentru GPA, PAM şi
GEPA sunt respectiv 2,1 – 14,4, 2,4 – 10,1 şi 0,5 – 3,7/milion, prevalenţa vasculitelor ANCA pozitive
fiind de 46 – 184/milion. Ratele de supravieţuire la 5 ani pentru GPA, PAM şi GEPA sunt estimate a fi
respectiv 74 – 91%, 45 – 76% şi 60 – 97%.
II. DIAGNOSTIC/EVALUARE
II.1. Diagnostic
Având în vedere că actualmente nu există criterii de clasificare sau de diagnostic validate pentru
vasculitele ANCA pozitive şi că ANCA nu au specificitate de 100% pentru vasculitele ANCA pozitive,
diagnosticul pozitiv al vasculitelor ANCA pozitive rămâne încă o provocare.
Diagnosticul pozitiv al vasculitelor ANCA pozitive se bazează pe identificarea ANCA fie prin
IFI pe substrat neutrofilic, de tip citoplasmatic (c-ANCA) sau de tip perinuclear (p-ANCA), sau prin
metoda ELISA de tip PR3-ANCA sau de tip MPO-ANCA în asociere cu variate simptome/semne
clinice şi investigaţii paraclinice inclusiv de tip imagistic evocatoare pentru diagnosticul pozitiv al
acestui grup de boli. Biopsia tisulară (renală, pulmonară, cutanată, sinusală etc.) cu identificarea
glomerulonefritei pauci-imune sau vasculitei necrotice a vaselor mici sau medii cu sau fără evidenţiere
de granuloame peri sau extravasculare reprezintă “standardul de aur” în diagnosticul pozitiv al
vasculitelor ANCA pozitive.
II.2. Evaluare
– Evaluarea vasculitelor ANCA pozitive implică evaluarea activităţii bolii, evaluarea afectării
structurale a diverselor organe şi sisteme afectate şi evaluarea stării de sănătate.
– Evaluarea activităţii bolii în vasculitele ANCA pozitive se bazează pe Birmingham Vasculitis
Activity Score (BVAS), versiunea 3, care cuprinde 9 domenii cu 56 elemente (v. Anexa 1).
Scorul BVAS variază de la 0 la 56, scorurile cele mai mari indicând boală activă sever, pe când
scorurile mai mici indică boală mai puţin activă.
– Evaluarea afectării structurale în vasculitele ANCA pozitive se bazează pe Vascular Damage
Index (VDI) care cuprinde 11 domenii cu 64 de elemente (v. Anexa 2). Scorul VDI variază de la
0 la 64, scorurile cele mai mari indicând boală distructivă sever, pe când scorurile mai mici
indică boală mai puţin distructivă, fără a putea discerne între manifestările structurale produse de
vasculită sau de toxicitatea medicamentoasă.
– Evaluarea stării de sănătate se bazează pe EQ-5D-3L (v. Anexa 3).
III. TRATAMENT
III.1. Principii terapeutice
Având în vedere caracterul intens distructiv al leziunilor tisulare care caracterizează acest grup
de boli este important de subliniat faptul că toate formele de boală necesită tratament, selecţia terapiilor
fiind făcută în funcţie de forma de boală, terapiile anterioare, complicaţiile induse de boală sau de
tratament şi caracteristicile individuale ale pacientului.
Terapia actuală a vasculitelor ANCA pozitive a scăzut major rata morbidităţii şi mortalităţii în
acest grup de boli, transformându-le din boli potenţial fatale fără tratament în boli cronice, cu remisiuni
şi recăderi sub tratament.
Având în vedere prevalenţa crescută a GPA şi a PAM versus GEPA, în ciuda suprapunerii
elementelor clinice, caracteristicilor histologice şi a posibilităţilor evolutive, eforturile terapeutice sunt
actualmente concentrate asupra primelor 2 forme de vasculite integrate în grupul vasculitelor ANCA
pozitive.
Tratamentul vasculitelor ANCA pozitive cuprinde următoarele tipuri de abordare terapeutică:
– terapia de inducţie a remisiunii cu durată de 3 – 6 luni, efectuată cu scopul de inhibiţie rapidă
a inflamaţiei organelor şi sistemelor afectate, se realizează cu imunosupresoare
(ciclofosfamidă/CF) sau biologice (rituximab/RTX) în asociere cu glucocorticoizi iniţial în
doze mari, ulterior cu scăderea progresivă a dozelor (“tapering”) până la discontinuarea lor.
“Ţinta terapiei de inducţie” la 3 – 6 luni este reprezentată de inhibiţia inflamaţiei organelor şi
sistemelor afectate în absenţa terapiei cu glucocorticoizi; remisiunea completă semnifică la 6
luni boala inactivă cu BVAS = 0 în absenţa tratamentului cu glucocorticoizi, iar remisiunea
incompletă semnifică la 6 luni boala inactivă cu BVAS = 0 în prezenţa tratamentului cu
glucocorticoizi în doză mică (prednison ≤ 10 mg/zi).
Selecţia terapiei imunosupresoare sau biologice de inducţie a remisiunii se bazează pe forma clinică de
boală; astfel, pacienţii cu boală ameninţătoare de organ se tratează cu CF sau RTX, la care se asociază
plasmafereză în situaţia pacienţilor cu manifestări ameninţătoare de viaţă (insuficienţă renală rapid
progresivă, hemoragie pulmonară), pe când pacienţii fără boală ameninţătoare de organ se tratează cu
metotrexat (MTX) sau micofenolat mofetil (MFM) în asociere cu glucocorticoizii în schema prezentată
anterior.
– terapia de menţinere a remisiunii cu durată de aproximativ 2 – 3 ani efectuată cu scopul de a
menţine inhibiţia inflamaţiei organelor şi sistemelor afectate în vederea diminuării “damageului” tisular indus de boală sau de tratament, se realizează cu imunosupresoare sau biologice
(RTX) selecţionate după tipul de medicament cu care s-a realizat inducţia remisiunii: astfel,
pacienţii la care remisiunea s-a obţinut cu CF şi glucocorticoizi pot fi trecuţi pe azatioprină
(AZA) sau metotrexat (MTX), pacienții la care remisiunea s-a obținut cu RTX și
glucocorticoizi pot fi trecuți pe RTX.
“Ţinta terapiei de menţinere a remisiunii” la 2 – 3 ani este reprezentată de inhibiţia inflamaţiei organelor
şi sistemelor afectate răspunzătoare de “damage” tisular în absenţa terapiei cu glucocorticoizi şi
imunosupresoare sau biologice.
– terapia recăderilor care apar frecvent (50%) în cursul terapiei de menţinere a remisiunii şi care
se asociază cu creşterea BVAS cu 1 punct sau mai mult se realizează cu reluarea schemei de
terapie de inducţie a remisiunii cu imunosupresoare sau biologice în asociere cu
glucocorticoizi iniţial în doze mari, ulterior cu scăderea progresivă a dozelor (“tapering”) până
la discontinuarea lor. Este cunoscut faptul că RTX este mai eficace comparativ cu CF în
tratamentul recăderilor.
– terapia formelor rezistente la CF: deşi CF reprezintă standardul terapiei în vasculitele ANCA
pozitive, aproximativ 15% dintre pacienţi nu răspund la CF; se defineşte prin absenţa scăderii
BVAS cu 1 punct sau apariţia unei noi manifestări a bolii. Tratamentul cu RTX este o
abordare terapeutică mai eficientă şi mai sigură în această situaţie.
III.2. Locul rituximabului (original şi biosimilar) în tratamentul vasculitelor ANCA pozitive
Rituximab (RTX) este un anticorp monoclonal chimeric anti-CD20 de pe suprafaţa limfocitelor B,
inducând depleţia celulelor B implicate în producţia de autoanticorpi cum sunt ANCA.
Actualmente, în conformitate cu studiile internaţionale controlate, RTX este indicat atât în terapia de
inducţie a remisiunii cât și în terapia de menținere a remisiunii la pacienţii cu granulomatoză cu
poliangiită (GPA) şi poliangiita microscopică (PAM) sever active.
III.2.1. Criteriile de includere a pacienţilor cu GPA şi PAM în tratamentul cu RTX (original și
biosimilar)
Pentru includerea unui pacient cu GPA sau PAM în terapia biologică cu RTX (original și biosimilar)
este necesară îndeplinirea cumulativă a următoarelor criterii:
1. vârsta peste 18 ani;
2. confirmarea diagnosticului de vasculită ANCA pozitivă:
– pozitivitate pentru ANCA prin IFI pe substrat neutrofilic, de tip citoplasmatic (c-ANCA)
sau de tip perinuclear (p-ANCA) sau prin metoda ELISA de tip PR3-ANCA sau de tip
MPO-ANCA în orice titru anormal (peste valoarea de referinţă a laboratorului), cu
documentaţie doveditoare, evaluare efectuată cu maximum 30 de zile înainte de indicarea
terapiei cu RTX;
– combinaţie de simptome/semne şi teste paraclinice caracteristice pentru diagnosticul
pozitiv de GPA şi PAM cu documentaţie doveditoare, evaluare efectuată cu maximum 30
de zile înainte de indicarea terapiei cu RTX;
Pentru pacienţii cu GPA se utilizează criteriile ACR de clasificare a bolii din 1990 (v.
Anexa4).
– biopsie tisulară (renală, pulmonară cutanată, sinuzală etc.) cu prezenţa de glomerulonefrită
pauci-imună sau vasculită necrotică a vaselor mici şi/sau granuloame perivasculare sau
extravasculare (cu documentaţie doveditoare) numai în situaţia când este posibilă
efectuarea ei;
3. confirmarea gradului de activitate al bolii:
– forme sever active de GPA şi PAM de tip boală ameninţătoare de organ sau boală
ameninţătoare de viaţă (afectare renală severă şi progresivă; afectare pulmonară severă şi
progresivă inclusiv hemoragie alveolară; afectare gastrointestinală, cardiacă, nervoasă şi
oculară severă şi progresivă; orice manifestare considerată destul de severă ca să necesite
tratament de inducţie a remisiunii) cu BVAS ≥ 3.
– asociate cu una dintre următoarele condiţii:
4. contraindicaţii/intoleranţă la tratamentul cu CF; de exemplu, conform rezumatului
caracteristicilor produsului:
– hipersensibilizare la CF;
– deteriorare severă a funcţiei măduvei osoase în special la pacienţii care au făcut pretratament cu medicamente citotoxice mielosupresoare sau radioterapie;
– cistită şi obstrucţie a tractului urinar;
sau
5. forme de boală rezistente la CF care nu au atins remisiunea în 3 – 6 luni de tratament cu CF (cu
documentaţie doveditoare).
Sau
6. tratamentul ulterior cu CF ar depăşi doza cumulativă maximă (25 g) stabilită de producător.
Sau
7. antecedente de carcinom uro-epitelial
sau
8. la pacienţi cu potenţial reproductiv, în vederea prezervării rezervei ovariene sau testiculare
pentru procreere.
III.2.2. Screening-ul necesar anterior iniţierii terapiei biologice în vasculitele ANCA pozitive
III.2.2.1. Tuberculoza
Înaintea iniţierii terapiei biologice cu RTX în vasculitele ANCA pozitive se va evalua riscul pacientului
de a dezvolta o reactivare a unei tuberculoze latente, în condiţiile în care este cunoscută imunodepresia
acestor pacienţi indusă de boală sau tratamente. Evaluarea riscului de tuberculoză va cuprinde:
anamneză, examen clinic, radiografie pulmonară şi teste de tip IGRA (interferon-gamma release assays):
QuantiFERON TB Gold sau testul cutanat la tuberculină (TCT). Pentru pacienţii testaţi pozitiv la
QuantiFERON sau la TCT (TCT ≥ 5 mm) se indică consult pneumologic în vederea chimioprofilaxiei
(efectuată sub supravegherea medicului pneumolog; terapia biologică se poate iniţia după minimum o
lună de tratament profilactic, numai cu avizul expres al medicului pneumolog). Numai la pacienţii care
au avut teste iniţiale negative, se recomandă repetarea periodică a screening-ului pentru reactivarea
tuberculozei (inclusiv testul QuantiFERON sau TCT), în caz de necesitate dar nu mai rar de un an (la
reevaluare se va folosi acelaşi test care a fost folosit iniţial).
III.2.2.2. Hepatitele virale
Ţinând cont de riscul crescut al reactivării infecţiilor cu virusuri hepatitice B şi C, care pot îmbrăca
forme fulminante, deseori letale, este imperios necesar ca înaintea iniţierii terapiei biologice la pacienţii
cu vasculite ANCA pozitive să se efectueze screeningul infecţiilor cronice cu virusurile hepatitice B şi
C. Markerii serologici virali care trebuie obligatoriu solicitaţi alături de transaminase hepatice înainte de
iniţierea unei terapii biologice sunt pentru virusul hepatitic B (VHB): antigen HBs, anticorpi anti-HBs,
anticorpi anti-HBc (IgG); pentru virusul hepatitic C (VHC): anticorpi anti-VHC.
Decizia de iniţiere a terapiei biologice la cei cu markeri virali pozitivi impune avizul explicit al
medicului specialist în boli infecţioase sau gastroenterologie, care va efectua o evaluare completă
(hepatică şi virusologică) a pacientului şi va recomanda măsurile profilactice care se impun, stabilind
momentul când terapia biologică poate fi iniţiată, precum şi schema de monitorizare a siguranţei
hepatice. Se recomandă repetarea periodică a screening-ului pentru infecţiile cronice cu virusuri
hepatitice B şi C, în caz de necesitate, dar nu mai rar de un an.
III.2.3.1. Schema de administrare a rituximabului (original şi biosimilar) în terapia de inducţie a
remisiunii în GPA şi PAM sever active:
– 375 mg/m2 săptămânal intravenos timp de 4 săptămâni; premedicaţia cu antipiretice (exemplu:
paracetamol), antihistaminice (exemplu: difenhidramină) şi 100 mg metilprednisolon (cu 30
minute înaintea administrării de RTX) este obligatorie.
– precedat de
– pulsterapie cu metil prednisolon (1000 mg/zi), 1 – 3 zile consecutiv urmat de prednisone doză
mare (până la 1 mg/kg corp/zi) cu scăderea progresivă a dozelor (“tapering”) până la 5 mg/zi la 5
luni şi renunţarea la glucocorticoizi după 6 luni de tratament în vederea realizării “ţintei” terapiei
de inducţie a remisiunii.
Pentru profilaxia pneumoniei cu Pneumocystis jirovecii se recomandă tratament profilactic cu Biseptol
(trimethoprin 80 mg/sulfametoxazol 400 mg) 1 tabletă zilnic pentru 5 – 7 zile sau 2 tablete pe zi de trei
ori timp de o săptămână.
III.2.3.2. Schema de administrare a rituximabului (original și biosimilar) în terapia de menținere
a remisiunii în GPA și PAM sever active
– 2 perfuzii a 500 mg intravenos, separate printr-un interval de 2 saptamani, ulterior
administrându-se câte o perfuzie de 500 mg intravenos la interval de 24 săptămâni.
Administrarea rituximabului (original și biosimilar) se va face pe o perioadă de minimum 24 luni după
obținerea remisiunii (absența semnelor și simptomelor clinice). În cazul pacienților cu risc crescut de
recurență a bolii, medicul trebuie să ia în considerare prelungirea duratei terapiei de menținere a
remisiunii până la 5 ani.
După inducția remisiunii cu rituximab (original și biosimilar), tratamentul de menținere a remisiunii cu
rituximab (original și biosimilar) la pacienții adulți cu GPA și PAM nu trebuie inițiat la un interval mai
scurt de 16 săptămâni după ultima perfuzie de rituximab (original și biosimilar).
După inducția remisiunii cu alte tratamente imunosupresoare standard, tratamentul de menținere a
remisiunii cu rituximab (original și biosimilar) la pacienții adulți cu GPA și PAM trebuie inițiat în
interval de 4 săptămâni de la obținerea remisiunii.
III.2.4. Evaluarea răspunsului la tratamentul cu rituximab (original și biosimilar) în terapia de
inducţie a remisiunii în GPA şi PAM active sever
• Evaluarea răspunsului la tratamentul cu RTX (original și biosimilar) în terapia de inducţie a GPA
şi PAM active sever se face astfel:
– I evaluare la 8 săptămâni de la începerea terapiei cu RTX (original și biosimilar)
– a II-a evaluare la 16 săptămâni de la începerea terapiei cu RTX (original și biosimilar)
– a III-a evaluare la 24 săptămâni de la începerea terapiei cu RTX (original și biosimilar)
• Evaluarea răspunsului la tratament cu RTX (original și biosimilar) în terapia de inducţie a GPA
şi PAM active sever se face cu:
– examen clinic
– investigaţii biochimice (hemoleucograma, VSH, proteina C reactivă, uree, creatinină, acid uric,
examen sumar urină, proteinurie, clearance la creatinină).
– evaluarea activităţii bolii: BVAS = 0 fie în absenţa tratamentului cu glucocorticoizi (remisiune
completă) fie în prezenţa tratamentului cu glucocorticoizi în doză mică (prednison ≤ 10 mg/zi)
(remisiune incompletă).
– evaluarea “damage-ului” indus de boală sau tratament: VDI
– evaluarea stării de sănătate: EQ-5D-3L
– determinarea ANCA (PR3-ANCA, MPO-ANCA) la 24 săptămâni
III.2.4.1. Evaluarea răspunsului la tratamentul cu rituximab (original și biosimilar) în terapia de
menținere a remisiunii în GPA și PAM active sever
• Evaluarea răspunsului la tratamentul cu RTX (original și biosimilar) în terapia de menținere a
remisiunii a GPA și PAM se face la 24 săptămâni
• Evaluarea răspunsului la tratamentul cu RTX (original și biosimilar) în terapia de menținere a
remisiunii a GPA și PAM se face cu:
– examen clinic
– investigaţii biochimice (hemoleucograma, VSH, proteina C reactivă, uree, creatinină, acid uric,
examen sumar urină, proteinurie, clearance la creatinină).
– evaluarea activităţii bolii: BVAS = 0 fie în absenţa tratamentului cu glucocorticoizi (remisiune
completă) fie în prezenţa tratamentului cu glucocorticoizi în doză mică (prednison ≤ 10 mg/zi)
(remisiune incompletă).
– evaluarea “damage-ului” indus de boală sau tratament: VDI
– evaluarea stării de sănătate: EQ-5D-3L
– determinarea ANCA (PR3-ANCA, MPO-ANCA) la 24 săptămâni
III.2.5. Contraindicaţii şi criterii de excludere a rituximabului (original și biosimilar) din
tratamentul vasculitelor ANCA pozitive
1. pacienţi cu infecţii severe (actuale, netratate) precum (dar nu limitativ): stări septice, abcese,
tuberculoză activă, infecţii oportuniste sau orice alte infecţii considerate semnificative în opinia
medicului curant.
2. pacienţii cu hepatite virale B sau C, infecţia cu HIV sau orice alte infecţii considerate
semnificative în opinia medicului curant.
3. pacienţii cu infecţii cronice active cu VHB şi utilizat cu prudenţă la cei cu infecţie cronică VHC,
cu monitorizare atentă. În ambele situaţii de infecţie virală B sau C decizia de iniţiere şi
continuare a terapiei impune avizul medicului infecţionist sau gastroenterolog;
4. pacienţi cu hipogammaglobulinemie (IgG seric < 400 mg/dL) sau deficienţă de IgA (IgA seric <
10 mg/dL).
5. pacienţi cu transplant de organ sau transplant de măduvă sau celule stem hematopoietice.
6. hipersensibilitate sau alergie la RTX sau la orice component din preparat.
7. sarcina şi alăptarea.
8. pacienţi cu stări de imunodeficienţă severă.
9. administrarea vaccinurilor cu germeni vii concomitent cu RTX în ultimele 30 de zile.
10. afecţiuni maligne prezente sau afecţiuni maligne în ultimii 5 ani, fără avizul medicului oncolog.
11. orice contraindicaţii menţionate de rezumatul caracteristicilor produsului.
12. atenţionări: pacienţii care se prezintă cu semne neurologice noi sau cu deteriorarea semnelor şi
simptomelor preexistente în cursul tratamentului cu RTX trebuie evaluaţi pentru
leucoencefalopatie progresivă multifocală (LMF).
13. lipsa/retragerea consimţământului pacientului faţă de tratament.
14. pierderea calităţii de asigurat.
IV. Prescriptori
Medicul de specialitate (reumatologie, nefrologie, medicină internă, pneumologie) care are dreptul de a
prescrie tratament specific în conformitate cu Hotărârea Guvernului nr. 720/2008 pentru aprobarea
Listei cuprinzând denumirile comune internaţionale corespunzătoare medicamentelor de care
beneficiază asiguraţii, cu sau fără contribuţie personală, pe bază de prescripţie medicală, în sistemul de
asigurări sociale de sănătate, precum şi denumirile comune internaţionale corespunzătoare
medicamentelor care se acordă în cadrul programelor naţionale de sănătate, cu modificările şi
completările ulterioare, va completa o foaie de observaţie clinică generală/fişă medicală care va conţine
evaluările clinice şi de laborator, imagistice şi histologice necesare, datele fiind introduse în aplicaţia
informatică a Registrului Român de Boli Reumatice (RRBR).
Se recomandă înregistrarea următoarelor date, atât la iniţierea terapiei, cât şi pe parcursul evoluţiei bolii
sub tratament:
– date generale legate de pacient
– date socio-demografice (vârstă, sex, status reproductiv, fumător/nefumător etc.)
– date legate de vasculită
• tipul de vasculită ANCA pozitivă (GPA, PAM, GEPA)
• tipul de ANCA (PR3-ANCA, MPO-ANCA)
– date legate de boală
• boală nou diagnosticată
• boală cu recădere
• boală cu afectare renală severă (cilindri, glomerulonefrită confirmată histologic, creşterea
screatininei cu > 30%)
• boală cu afectare pulmonară severă sau hemoragie alveolară difuză
– antecedente patologice/comorbidităţi
– medicaţie
– status pulmonar (rezultatul testului QuantiFERON/TB Gold sau testului cutanat la tuberculină,
avizul medicului pneumolog în cazul unui rezultat pozitiv) sau hepatic (rezultatele testelor pentru
hepatitele virale B şi C, avizul medicului gastroenterolog sau infecţionist în cazul unui rezultat
pozitiv)
– evaluarea activităţii bolii conform cu BVAS.
– evaluarea afectării structurale a bolii conform cu VDI;
– evaluarea stării de sănătate actuale a pacientului conform cu EQ-5D-3L
– bilanţ biologic
– justificarea recomandării tratamentului cu RTX (verificarea îndeplinirii criteriilor de protocol);
– preparatul biologic recomandat: denumirea comună internaţională şi denumirea comercială,
precizând doza şi schema terapeutică;
Pentru iniţierea terapiei biologice cu RTX (original si biosimilar) se recomandă obţinerea unei a doua
opinii de la un medic primar în specialitatea reumatologie, sau nefrologie, sau medicină internă sau
pneumologie dintr-un centru universitar (Bucureşti, Iaşi, Cluj, Târgu Mureş, Constanţa, Craiova,
Timişoara) privind diagnosticul, gradul de activitate al bolii şi necesitatea instituirii tratamentului
biologic cu RTX (original și biosimilar). Medicul care oferă a doua opinie va utiliza aceleaşi criterii de
protocol ca şi medicul prescriptor care iniţiază şi supraveghează tratamentul cu RTX (original și
biosimilar).
Medicul curant are obligaţia să discute cu pacientul starea evolutivă a bolii, prognosticul şi riscurile de
complicaţii, justificând indicaţia de tratament biologic. Vor fi detaliate atât beneficiile previzibile, cât şi
limitele şi riscurile potenţiale ale acestei terapii, vor fi discutate diversele variante de tratament
disponibil (preparate şi scheme terapeutice), precum şi monitorizarea necesară, astfel încât pacientul să
fie complet informat asupra tuturor aspectelor legate de tratamentul biologic recomandat. Medicul
curant va solicita pacientului să semneze o declaraţie de consimţământ informat privind tratamentul
recomandat, care va include în clar denumirea comună internaţională şi numele comercial al
preparatului recomandat şi va fi semnată şi datată personal de către pacient. Consimţământul este
obligatoriu la iniţierea tratamentului biologic precum şi pe parcursul acestuia, dacă pacientul trece în
grija altui medic curant. Medicul curant are obligaţia de a păstra originalul consimţământului informat.
Anexa Nr. 1
Birmingham Vasculitis Activity Score – versiunea 3 (BVAS3)
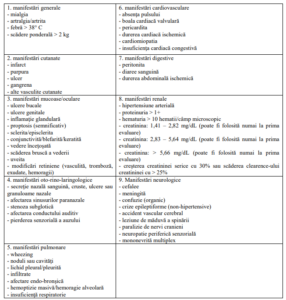
Anexa Nr. 2
Vasculitis Damage Index (VDI)

Anexa Nr. 3
Chestionarul EQ-5D-3L
Pentru fiecare întrebare de mai jos, vă rugăm să bifaţi un singur răspuns care vă descrie cel mai bine
starea dumneavoastră de sănătate astăzi.
Mobilitate
|¯| Nu am probleme în a mă deplasa
|¯| Am unele probleme în a mă deplasa
|¯| Sunt obligat/ă să stau în pat
Propria îngrijire
|¯| Nu am nicio problemă în a-mi purta singur/ă de grijă
|¯| Am unele probleme cu spălatul sau îmbrăcatul
|¯| Sunt incapabil/ă să mă spăl sau să mă îmbrac singur/ă
Activităţi obişnuite (de ex.: serviciu, studiu, gospodărie, activităţi în familie, timp liber)
|¯| Nu am probleme în îndeplinirea activităţilor mele obişnuite
|¯| Am unele probleme în îndeplinirea activităţilor mele obişnuite
|¯| Sunt incapabil/ă să-mi îndeplinesc activităţile mele obişnuite
Durere/Stare de disconfort
|¯| Nu am dureri sau stare de disconfort
|¯| Am dureri sau o stare de disconfort moderate
|¯| Am dureri sau o stare de disconfort extrem de puternice
Nelinişte/Deprimare
|¯| Nu sunt neliniştit/ă sau deprimat/ă
|¯| Sunt moderat neliniştit/ă sau deprimat/ă
|¯| Sunt extrem de neliniştit/ă sau deprimat/ă

Pentru a ajuta oamenii să spună cât de bună sau de rea este starea lor de sănătate, am desenat o scară (ca
un termometru) pe care starea cea mai bună pe care v-o puteţi imagina este marcată 100, iar cea mai rea
stare de sănătate pe care v-o puteţi imagina este marcată cu 0.
Vă rugăm să indicaţi pe această scară cât de bună sau de rea este sănătatea dumneavoastră astăzi, în
opinia dumneavoastră. Vă rugăm să faceţi acest lucru cu un X pe scara din dreapta.
Anexa Nr. 4
Criterii de clasificare pentru granulomatoza cu poliangiita (GPA)

Autor: FormareMedicala.ro









