Date despre hemofilia A congenitală:
Hemofilia A este o afecțiune hemoragică congenitală transmisă ereditar X-linkat, caracterizată
prin sinteza cantitativ diminuată sau calitativ alterată a factorului de coagulare VIII și care se
caracterizează prin sângerări spontane sau traumatice.
Conform datelor Federației Mondiale de Hemofilie (WFH) și ale Consorțiului European de
Hemofilie (EHC), nu există diferențe notabile ale incidenței hemofiliei congenitale, legate de
zona geografică, rasă sau de nivelul socio-economic.
Prevalența bolii este de aproximativ 25 de cazuri la 100.000 persoane de sex masculin, respectiv
1 bolnav la 10.000 persoane din populația totală. În medie, 80-85% din cazuri sunt reprezentate
de hemofilia A iar proporția formelor severe (nivelul FVIII<1%) este de 50-70%.
Complicații ale hemofiliei:
Expunerea la concentratele de factor VIII este asociată cu dezvoltarea de aloanticorpi
neutralizanți anti factor-VIII (inhibitori), care reduc efectul hemostatic al concentratelor de FVIII,
astfel încât tratamentul devine ineficient. Incidenţa inhibitorilor este de aproximativ 15-30% la
pacienţii cu hemofilie A.
Apariția anticorpilor anti factor-VIII este una dintre cele mai serioase complicații ale terapiei de
substituție la pacienții cu hemofilie congenitală.
Inhibitorii apar cel mai frecvent la pacienţii cu forme severe de boală comparativ cu cei care au
forme ușoare sau moderate de hemofilie A. Controlul sângerărilor este o mare provocare la
pacientii cu hemofilia A și inhibitori în comparație cu cei fără inhibitori. Inhibitorii de factor VIII
au un risc crescut de complicații musculoscheletale, durere, limitari din punct de vedere fizic care
pot impacta major calitatea vieții.
DCI EMICIZUMAB este un anticorp monoclonal umanizat modificat de tip imunoglobulină G4
(IgG4), cu structură de anticorp bispecific, indicat ca tratament profilactic de rutină pentru
prevenirea sângerărilor sau pentru reducerea frecvenței episoadelor de sângerare la pacienții cu
hemofilie A, care prezintă inhibitori de factor VIII Emicizumab se leagă simultan de factorul IX
activat și de factorul X, reconstituind astfel funcția factorului VIII activat deficitar, care este
necesar pentru o hemostază eficientă.
Emicizumab nu prezintă nicio conexiune structurală sau omologie secvenţială cu factorul VIII şi,
prin urmare, nu induce sau stimulează dezvoltarea de inhibitori ai factorului VIII.
I. Indicaţia terapeutică (face obiectul unui contract cost-volum):
1. Emicizumab este indicat ca tratament profilactic de rutină pentru prevenirea sângerărilor sau
pentru reducerea frecvenței episoadelor de sângerare la pacienții cu hemofilie A, care prezintă
inhibitori de factor VIII.
2. Emicizumab este indicat ca tratament profilactic de rutină pentru prevenirea sângerărilor sau
reducerea frecvenței episoadelor de sângerare la pacienții cu hemofilie A severă (deficienţă
congenitală de factor VIII, FVIII < 1%) care nu prezintă inhibitori de factor VIII.
II. Criterii de includere:
1. Hemofilia A cu inhibitori de FVIII: pacienți din toate grupele de vârstă (copii, adolescenți
și adulți), cu hemofilie A congenitală:
● care prezintă inhibitori de FVIII, nou diagnosticați sau
● care prezintă inhibitori de FVIII, cărora li s-a administrat anterior tratament episodic („la
nevoie”) sau profilactic cu agenți de bypass (CCPa și rFVIIa).
2. Hemofilia A fără inhibitori de FVIII: pacienți din toate grupele de vârstă (copii, adolescenți
și adulți), cu hemofilie A congenitală severa (FVIII < 1%):
● care nu prezintă inhibitori de FVIII, nou diagnosticați sau
● care nu prezintă inhibitori de FVIII, cărora li s-a administrat anterior tratament episodic („la
nevoie”) sau profilactic cu concentrate de factor VIII.
III. Criterii de excludere:
Hipersensibilitate la substanţa activă sau la oricare dintre excipienţii enumeraţi: L-arginină,
Lhistidină, L-acid aspartic, poloxamer 188, apă pentru preparate injectabile.
IV. Tratament:
Recomandări pentru inițierea tratamentului cu emicizumab:
Tratamentul (inclusiv profilaxia de rutină) cu substanţe hemostatice de bypassing (de exemplu
CCPa şi rFVIIa) trebuie întrerupt în ziua precedentă iniţierii terapiei cu emicizumab.
Profilaxia cu factor VIII poate fi continuată în primele 7 zile ale tratamentului cu emicizumab.
Emicizumab este destinat exclusiv utilizării subcutanate şi trebuie administrat cu
respectarea tehnicilor adecvate de asepsie.
Doze:
Doză de încărcare:
3 mg/kg o dată pe săptămână în primele 4 săptămâni.
Schema terapeutică a dozei de încărcare este aceeași, indiferent de schema terapeutică a dozei de
întreținere.
Doza de întreținere:
1,5 mg/kg o dată pe săptămână, sau
3 mg/kg la fiecare două săptămâni, sau
6 mg/kg la fiecare patru săptămâni.
Schema terapeutică a dozei de întreținere trebuie aleasă pe baza preferințelor medicului și a
pacientului/aparținătorului acestuia pentru a îmbunătăţi aderenţa la tratament.
Calcularea dozelor:
Doza (exprimată în mg) şi volumul (exprimat în ml) necesare pentru fiecare pacient trebuie
calculate după cum urmează:
• Doza de încărcare (3 mg/kg) o dată pe săptămână pentru primele 4 săptămâni:
Greutatea corporală a pacientului (kg) x doza (3 mg/kg) = cantitatea totală (mg) de emicizumab
care trebuie administrată
• Urmată de o doză de întreţinere fie de 1,5 mg/kg o dată pe săptămână, fie de 3 mg/kg la
fiecare două săptămâni sau de 6 mg/kg la fiecare patru săptămâni, începând cu săptămâna
5:
Greutatea corporală a pacientului (kg) x doza (1,5 mg/kg, 3 mg/kg sau 6 mg/kg) = cantitatea
totală (mg) de emicizumab care trebuie administrată
• Volumul total de emicizumab care trebuie administrat subcutanat trebuie calculat după
cum urmează:
– Cantitatea totală (mg) de emicizumab care trebuie administrată ÷ concentraţia
flaconului (mg/ml) = volumul total de emicizumab (ml) care trebuie administrat.
Nu trebuie combinate în aceeași seringă diferite concentraţii de emicizumab (30 mg/ml şi 150
mg/ml) atunci când se constituie volumul total care trebuie administrat.
Nu trebuie administrat un volum mai mare de 2 ml per injecţie.
Durata tratamentului:
Emicizumab este destinat tratamentului profilactic pe termen lung.
Ajustări ale dozei pe durata tratamentului:
Nu există recomandări privind ajustările dozei de emicizumab.
Omiterea sau întârzierea administrării dozelor:
Dacă pacientul omite să administreze una dintre injecţiile subcutanate de emicizumab
programate, acesta trebuie instruit să administreze doza omisă cât mai curând posibil, până la o zi
înainte de ziua programată pentru administrarea dozei următoare. Pacientul va administra doza
următoare conform programului obişnuit de administrare. Pacientul nu trebuie să administreze
două doze în aceeași zi pentru a compensa doza omisă.
V. Monitorizarea (clinică și de laborator) tratamentului cu emicizumab:
Pe baza studiilor preclinice, există posibilitatea apariţiei fenomenului de hipercoagulare în cazul
administrării de rFVIIa sau FVIII în asociere cu emicizumab. Emicizumab creşte potenţialul de
coagulare, prin urmare doza de FVIIa sau FVIII necesară pentru a atinge hemostaza poate fi mai
mică în cazul în care se administrează tratament profilactic cu emicizumab.
Experienţa în cazul administrării concomitente de medicamente antifibrinolitice şi CCPa sau
rFVIIa la pacienţii cărora li se administrează tratament profilactic cu emicizumab este limitată.
Cu toate acestea, trebuie să se ia în considerare posibilitatea apariţiei de evenimente trombotice în
cazul în care medicamentele antifibrinolitice sunt utilizate în asociere cu CCPa sau rFVIIa la
pacienţii trataţi cu emicizumab.
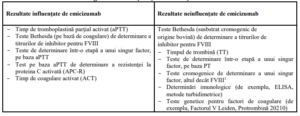
Testele de laborator care sunt sau nu sunt influenţate de prezenţa emicizumab, sunt menţionate în
tabelul de mai jos. Din cauza timpului de înjumătăţire plasmatică prelungit, aceste efecte asupra
testelor de coagulare pot persista timp de până la 6 luni după administrarea ultimei doze.
Rezultate ale testelor de coagulare influenţate şi neinfluenţate de emicizumab
VI. Recomandări pentru gestionarea sângerărilor acute (spontane)
1. Pacienți cu hemofilie A și inhibitori de factor VIII
În ciuda eficacității ridicate în prevenirea evenimentelor de sângerare, mai pot apărea evenimente
de sângerare spontană la pacienții cu profilaxie cu emicizumab, ceea ce pentru această categorie
de pacienți va însemna probabil, necesitatea utilizării concomitente a terapiilor hemostatice
alternative.
a. Abordarea generală a sângerărilor spontane: emicizumab este foarte probabil să transforme
fenotipul sângerării într-unul mai puțin sever. Dată fiind ameliorarea hemostazei la pacienții
tratați cu emicizumab în profilaxie, abordarea curentă de a trata la primele semne și simptome de
sângerare, trebuie să se schimbe pentru unele cazuri. Sângerările semnificative și severe sau cele
amenințătoare de viață, în continuare trebuie tratate prompt. Cu toate acestea, este necesară o
evaluare suplimentară a acuzelor articulare și musculare înaintea tratamentului cu un agent
hemostatic suplimentar.
b. Precauții privind doza și durata terapiei cu agenți de bypass:
• Episoadele de sângerare acută se pot trata cu Factor VII de coagulare activat
recombinant (rFVIIa) cu o doză de 90-120 μg/kg, ca doză inițială. Marea majoritate a
sângerărilor ar putea fi tratate cu 1-3 doze, administrate la intervale de 2 ore.
• Administrarea de CCPa pentru sângerările spontane la pacienții aflați în tratament
cu emicizumab ar trebui evitată, iar rFVIIa ar trebui să fie prima opțiune pentru
tratament.
• Dacă se administrează CCPa, doza nu va trebui să fie mai mare de 50 U/kg ca doză inițială
și nu va depăși 100 U/kg/zi. Durata terapiei cu CCPa trebuie minimizată, existând riscul de
apariție a trombozei și a microangiopatiei trombotice la administrarea pe perioade mai mari
de 24 ore, în special cu doze de peste 100 U/kg/zi.
• Dozele repetate de agenți de bypass, oricare dintre ei ar fi utilizat, dincolo de
recomandările de mai sus, se fac sub supravegherea medicului, luând în considerare
evaluarea severității sângerărilor înainte de a se repeta dozele.
• Pentru sângerările semnificative care nu răspund la agenții de bypass, se va lua în
considerare utilizarea de factor VIII de origine porcină sau factor VIII uman dacă
este parțial tolerat. Utilizarea acestor agenți permite de asemenea monitorizarea
terapeutică cu ajutorul testelor cromogenice cu substrat de origine bovină.
2. Pacienți cu hemofilie A severa fără inhibitori de factor VIII
În ciuda eficacității ridicate în prevenirea evenimentelor hemoragice, mai pot apărea episoade de
sângerare acută la pacienții tratați cu profilaxie cu emicizumab, ceea ce, în cazul pacienților cu
hemofilie A fără inhibitori, va însemna probabil necesitatea utilizării concomitente a terapiei de
substituție cu factor FVIII. Nu au fost observate evenimente adverse grave legate de utilizarea
concomitentă a concentratelor de FVIII la pacienții aflați în profilaxie cu emicizumab. Mai exact,
nu au fost observate evenimente trombotice sau de microangiopatie trombotică. Mai jos sunt
câteva recomandări specifice care trebuie luate în considerare în acest grup de pacienți.
a. Abordare generală a sângerării spontane: Emicizumab este probabil să transforme fenotipul
sângerării într-unul mai puțin sever, cu o reducere semnificativă a episoadelor hemoragice care
necesită tratament. Sângerările semnificative și severe sau cele amenințătoare de viață, în
continuare trebuie tratate prompt.
b. Toate concentratele de FVIII (cu timp de înjumătățire standard sau timp de înjumătățire
prelungit) pot fi utilizate pentru evenimentele de sângerare acută. Dozarea ar trebui să urmeze
aceleași recomandări ca atunci când pacientul se afla în terapie de substituție cu factor FVIII
(teste cromogenice de evaluare a FVIII).
VII. Recomandări privind managementul intervențiilor chirurgicale cu emicizumab
Siguranţa şi eficacitatea emicizumab nu au fost evaluate în mod formal în cazul intervenţiilor
chirurgicale. În studiile clinice, pacienţii au avut intervenţii chirurgicale fără întreruperea
tratamentului profilactic cu emicizumab.
Deși emicizumab ameliorează hemostaza, el nu o normalizează. Acest aspect important este de
reținut când se planifică un control hemostatic în cadrul unei intervenții chirurgicale. În cadrul
studiilor clinice, unii pacienți au prezentat un control al hemostazei adecvat doar cu emicizumab
pentru intervenții chirurgicale minore, în timp ce alții nu. Această situație este similară cu ceea ce
s-a observat în timp la pacienții cu hemofilie formă moderată.
• Intervențiile chirurgicale ar trebui să fie efectuate în centre cu experiență și cu acces la
testele necesare de laborator atunci când se utilizează în același timp și agenți hemostatici.
• Intervențiile chirurgicale la cerere ar trebui efectuate după ce pacienții au finalizat faza de
inițiere a tratamentului cu emicizumab și sunt în faza de menținere cu o doză fixă,
stabilită.
• Emicizumab în monoterapie – această abordare nu ar trebui să se presupună ca fiind
adecvată pentru cazul intervențiilor chirurgicale majore unde standardele actuale de
tratament sunt de a menține nivelurile de factor în limitele normale, pentru o perioadă de
mai multe zile.
• Monitorizarea îndeaproape a controlului sângerărilor, ca și accesul la teste specifice de
laborator pentru monitorizarea terapiei (ex. teste cromogenice de evaluare a FVIII cu
înlocuirea FVIII) sunt de o importanță maximă atunci când se decid planurile terapeutice
pentru pacienții tratați cu emicizumab ce au nevoie de proceduri chirurgicale.
• Pentru proceduri și intervenții chirurgicale majore unde sângerarea poate conduce
la complicații serioase, pacienților trebuie să li se administreze factor rFVIIa, pre și
post operator pentru a menține hemostaza în parametrii normali.
• Medicii sunt avertizați să ia în considerare faptul că complicațiile hemoragice cauzate de
intervențiile chirurgicale la pacienții cu hemofilie depășesc încă cu mult complicațiile
trombotice în frecvență și morbiditate / mortalitate.
VIII. Întreruperea tratamentului:
Pacienţii care urmează tratament profilactic cu emicizumab trebuie monitorizaţi pentru apariţia
evenimentelor de tromboembolism atunci când li se administrează concomitent CCPa.
Medicul trebuie să sisteze imediat administrarea CCPa şi să întrerupă terapia cu emicizumab în
cazul în care apar simptome clinice şi/sau rezultate ale analizelor de laborator sugestive pentru
microangiopatie trombotica (MAT) și să abordeze terapeutic cazul, după cum este indicat clinic.
IX. Reluare tratament:
După rezoluţia MAT, medicii şi pacienţii/aparţinătorii trebuie să analizeze, în funcţie de caz,
riscurile şi beneficiile reluării tratamentului profilactic cu emicizumab.
X. Prescriptori
Medici cu specialitatea hematologie, pediatrie sau medicină internă, cu atestare din partea unui
serviciu de hematologie, pentru cazurile în care nu există medic pediatru sau hematolog, din
unitățile sanitare prin care se deruleaza programul P6.27-Boli rare-medicamente incluse
conditionat( unitatile sanitare prin care se deruleaza si PNS hemofilie si talasemie).”
Autor: FormareMedicala.ro