I.Indicații
Elosulfase alfa este indicat pentru tratamentul mucopolizaharidozei tip IVA (sindromul Morquio A, MPS
IVA) la pacienţii de orice vârstă.
Mucopolizaharidozele sunt un grup de patologii rare, de origine genetică și cauzate de defecte
congenitale ale enzimelor lizozomale. Sunt heterogene din punct de vedere clinic și cu evoluție
progresivă.
Mucopolizaharidoza tip IVA (MPS IVA sau sindromul Morquio A) este una dintre aceste patologii,
transmisibilă pe cale autozomal recesivă și este cauzată de deficiența enzimei lizozomale N-acetylglucozamina-6-sulfataza (GALNS), ceea ce determină o acumulare sistemică de glicozaminoglicani (GAG)
parțial degradați de tipul keratan-sulfat (KS) şi condroitina-6-sulfat (C6S). Gena codanta (galns) se află pe
braţul lung al cromozomului 16 (16q24.3).
II. Tratament
Alfa elosulfaza o terapie de substituție enzimatică, este forma recombinantă a enzimei umane galns și
este primul medicament aprobat pentru tratamentul MPS IVA, pentru care doar tratamentul suportiv
este pentru moment disponibil. Tratamentul suportiv include medicație anti-inflamatorie nonsteroidiană și tratament chirurgical.
Acest medicament înlocuieşte enzima naturală N-acetilgalactozamină-6-sulfatază care lipseşte la
pacienţii cu MPS IVA. S-a demonstrat în urma studilor clinice că tratamentul îmbunătăţeşte mersul şi
scade valorile de keratan sulfat din organism. Acest medicament poate ameliora simptomele de MPS
IVA.
Tratamentul cu elosufase alfa trebuie supravegheat de un medic cu experienţă în gestionarea pacienţilor
cu MPS IVA sau alte boli metabolice ereditare. Administrarea trebuie să fie efectuată de către personal
medical instruit corespunzător care are capacitatea de a face faţă urgenţelor medicale.
Doze
Doza recomandată de alfa elosulfază este de 2 mg/kg de greutate corporală administrată o dată pe
săptămână. Volumul total al perfuziei trebuie administrat pe o durată de aproximativ 4 ore (vezi Tabelul
1).
Din cauza posibilelor reacţii de hipersensibilitate la alfa elosulfază, pacienţilor trebuie să li se
administreze antihistaminice cu sau fără antipiretice cu 30 – 60 de minute înainte de începerea perfuziei.
Populaţii speciale
– Vârstnici (≥ 65 de ani)
Siguranţa şi eficacitatea elosulfase alfa la pacienţii cu vârsta de peste 65 de ani nu au fost
stabilite şi nu se poate face nicio recomandare privind un regim alternativ de dozare la aceşti
pacienţi. Nu se cunoaşte dacă pacienţii vârstnici răspund diferit faţă de pacienţii tineri.
– Copii şi adolescenţi
Dozele la copii şi adolescenţi sunt la fel ca la adulţi. Datele disponibile în prezent sunt prezentate
in Tabel 1.
Mod de administrare: doar pentru perfuzie intravenoasă.
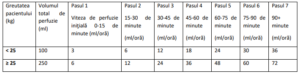
Pacienţilor care cântăresc mai puţin de 25 kg trebuie să li se administreze un volum total de 100 ml.
Atunci când este diluat în 100 ml, viteza de perfuzie iniţială trebuie să fie de 3 ml/oră. Viteza de perfuzie
poate fi crescută, în funcţie de toleranţă la fiecare 15 minute, după cum urmează: mai întâi se creşte
viteza la 6 ml/oră, apoi se creşte viteza la fiecare 15 minute cu creşteri de 6 ml/oră până când se atinge o
viteză maximă de 36 ml/oră.
Pacienţilor care cântăresc 25 kg sau mai mult trebuie să li se administreze un volum total de 250 ml.
Atunci când este diluat în 250 ml, viteza de perfuzie iniţială trebuie să fie de 6 ml/oră. Viteza de perfuzie
poate fi crescută în funcţie de toleranţă, la fiecare 15 minute, după cum urmează: mai întâi se creşte
viteza la 12 ml/oră, apoi se creşte viteza la fiecare 15 minute cu creşteri de 12 ml/oră până când se
atinge o viteză maximă de 72 ml/oră.
Tabelul 1: Volume şi viteze de perfuzie recomandate
Atenţionări şi precauţii speciale pentru utilizare
Anafilaxie şi reacţii alergice grave
S-au raportat anafilaxie şi reacţii alergice grave în cadrul studiilor clinice. Prin urmare, trebuie să fie
disponibil personal medical instruit corespunzător şi echipament adecvat atunci când se administrează
alfa elosulfază. În cazul în care apar aceste reacţii, se recomandă oprirea imediată a perfuziei şi iniţierea
unui tratament medical adecvat. Trebuie respectate standardele medicale în vigoare privind tratamentul
de urgenţă. La pacienţii care au manifestat reacţii alergice în timpul perfuziei, este necesară precauţie la
readministrare.
Reacţii legate de perfuzie
Reacţiile legate de perfuzie (infusion reactions, IR) au fost reacţiile adverse cel mai frecvent observate în
cadrul studiilor clinice. IR pot include reacţii alergice. Pacienţilor trebuie să li se administreze
antihistaminice cu sau fără antipiretice înainte de perfuzie. Gestionarea IR trebuie efectuată în funcţie de
gradul de severitate al reacţiei şi să includă încetinirea sau întreruperea temporară a perfuziei şi/sau
administrarea suplimentară de antihistaminice, antipiretice şi/sau corticosteroizi. Dacă apar IR grave, se
recomandă oprirea imediată a perfuziei şi iniţierea unui tratament adecvat. Readministrarea după o
reacţie gravă trebuie efectuată cu precauţie şi monitorizare atentă de către medicul curant.
Compresia măduvei spinării/cervicale
SCC (Spinal/Cervical cord compression [Compresia măduvei spinării/cervicale]) a fost observată atât la
pacienţii care au primit elosulfase alfa, cât şi la cei care au primit placebo în cadrul studiilor clinice.
Pacienţii trebuie monitorizaţi pentru depistarea semnelor şi simptomelor de SCC (incluzând dureri de
spate, paralizia membrelor sub nivelul compresiei, incontinenţă urinară şi a materiilor fecale) şi trebuie
să li se asigure tratamentul medical adecvat.
Dietă cu restricţie de sodiu
Acest medicament conţine 8 mg sodiu per flacon şi se administrează în soluţie pentru perfuzie de clorură
de sodiu 9 mg/ml (0,9%) Acest lucru trebuie avut în vedere la pacienţii care urmează o dietă cu restricţie
de sodiu.
Sorbitol
Pacienţii cu probleme ereditare rare de intoleranţă la fructoză nu trebuie să utilizeze acest medicament.
Fertilitatea, sarcina şi alăptarea
Pentru elosulfase alfa nu sunt disponibile date privind utilizarea la femeile gravide.
Ca măsură de precauţie, este de preferat să se evite utilizarea elosulfase alfa în timpul sarcinii, cu
excepţia cazurilor în care este absolut necesar.
Date disponibile privind reproducţia la animale au evidenţiat excreţia de alfa elosulfază în lapte. Nu se
cunoaşte dacă alfa elosulfaza se excretă în laptele uman, dar nu este de aşteptat expunerea sistemică
prin intermediul laptelui. Din cauza lipsei de date la oameni, elosulfase alfa trebuie administrat la femei
care alăptează doar dacă se consideră că beneficiul potenţial depăşeşte riscul potenţial pentru copil.
Nu s-a observat afectarea fertilităţii în cadrul studiilor non-clinice cu alfa elosulfază.
Efecte asupra capacităţii de a conduce vehicule şi de a folosi utilaje
elosulfase alfa are influenţă mică asupra capacităţii de a conduce vehicule sau de a folosi utilaje. S-au
raportat ameţeli în timpul perfuziilor; dacă ameţeala apare după perfuzie, poate fi afectată capacitatea
de a conduce vehicule şi de a folosi utilaje.
Reacţii adverse
Majoritatea reacţiilor adverse din cadrul studiilor clinice au fost IR, care sunt definite ca fiind reacţii
adverse apărute după iniţierea perfuziei şi până la sfârşitul zilei de perfuzie. IR grave au fost observate în
cadrul studiilor clinice şi au inclus anafilaxie, hipersensibilitate şi vărsături. Cele mai des întâlnite
simptome de IR (care au apărut la ≥ 10% dintre pacienţii trataţi cu Vimizim şi cu ≥ 5% mai mult în
comparaţie cu placebo) au fost dureri de cap, greaţă, vărsături, pirexie, frisoane şi dureri abdominale. IR
au fost în general uşoare sau moderate, iar frecvenţa a fost mai mare în primele 12 săptămâni de
tratament şi au avut tendinţa de a avea loc mai puţin frecvent în timp.
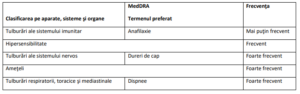
Datele din Tabelul 2 de mai jos descriu reacţiile adverse din cadrul studiilor clinice la pacienţii trataţi cu
elosulfase alfa.
Reacţiile adverse sunt definite în funcţie de frecvenţă astfel: foarte frecvente (≥ 1/10), frecvente (≥ 1/100
şi < 1/10), mai puţin frecvente (≥ 1/1000 şi < 1/100), rare (≥ 1/10000 şi < 1/1000), foarte rare (< 1/10000)
şi cu frecvenţă necunoscută (care nu poate fi estimată din datele disponibile). În cadrul fiecărei grupe de
frecvenţă, reacţiile adverse sunt prezentate în ordinea descrescătoare a gradului de severitate.
Tabelul 2: Reacţii adverse la pacienţii trataţi cu elosulfase alfa MedDRA

III. Prescriptori
Medici pediatri, Medicina Interna sau Reumatologie in cazul pacientilor adulti, neurologi, genetica
medicala din unitatile de specialitate prin care se deruleaza programul. Evaluare anuala a pacientilor in
Centrul de expertiza in boli metabolice lizozomale Cluj Napoca.
Autor: FormareMedicala.ro









